美国FDA新规5月15日生效:B2B官网须嵌入实时合规验证模块
2026年5月15日,美国食品药品监督管理局(FDA)正式实施《B2B数字合规声明指南》补充条款。该政策首次将企业官网的数字化合规呈现能力纳入供应链资质评估体系,直接影响中国对美出口医疗器械、食品接触材料及消费电子类产品的贸易准入效率与商业信任基础。
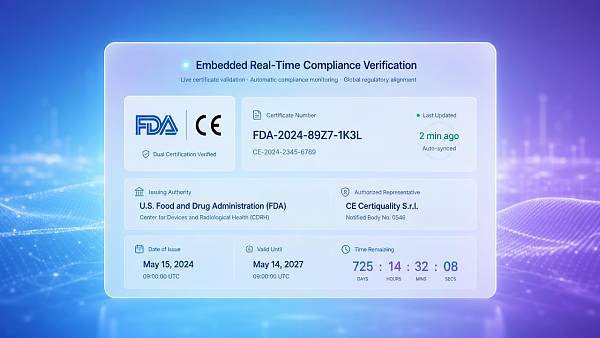
事件概述
美国FDA于2026年5月15日正式实施《B2B数字合规声明指南》补充条款,要求所有向美出口医疗器械、食品接触材料及消费电子类产品的中国供应商,其多语种官网必须集成可被FDA在线验证的结构化合规声明模块(含CE/FDA双标状态、证书编号、签发机构与有效期),否则将影响采购商在FDA Supplier Portal中的资质预审通过率。该要求直接影响海外进口商对供应商可信度评估与订单放行决策。
对哪些细分行业产生影响
直接贸易企业:作为FDA Supplier Portal中注册主体及采购合同签约方,其官网是进口商开展尽职调查的第一信息源。若未嵌入可验证模块,将导致资质预审延迟或标记为“信息不完整”,显著拉长新客户准入周期,并可能触发采购商要求提供第三方验证报告等额外成本。
原料采购企业:虽不直接出口成品,但其向下游制造商提供的关键原材料(如医用级硅胶、食品级PC树脂、RoHS合规芯片)需附具可追溯的合规证明。新规倒逼其官网同步升级声明模块,以支撑下游客户完成整机/整件合规披露义务,否则面临供应关系弱化风险。
加工制造企业:承担OEM/ODM角色的企业常以品牌方名义申报FDA列名,自身官网却长期缺失独立合规标识。新规实施后,进口商将更倾向选择具备自主合规数字基建能力的制造商,以降低连带责任风险;缺乏该能力者可能被排除在优质采购清单之外。
供应链服务企业:包括合规咨询、认证代办、数字平台开发等第三方服务商,其业务模式正从“单次证书服务”转向“持续性合规数据运维”。新规客观上加速了合规SaaS工具的市场渗透,也对服务商的数据结构化能力、API对接经验及多语种内容管理提出更高要求。
相关企业或从业者应关注重点及应对措施
确认官网是否满足结构化数据规范
需核查官网是否采用Schema.org标准中的Product与Certification扩展字段,支持FDA系统自动抓取证书编号、签发日期、有效期、认证机构URI等核心参数,而非仅静态展示PDF扫描件。
厘清多语种页面的合规声明一致性
英文主站与中文子站均须部署同等效力的验证模块;若仅英文页嵌入而中文页缺失,FDA系统可能判定为“信息不对称”,影响整体可信度评分。
建立证书动态更新机制
模块须与内部证书管理系统(如QMS)或认证机构数据库实现轻量级对接,确保证书过期、变更或撤销时,官网声明同步刷新,避免因信息滞后导致采购商误判。
预留FDA验证接口测试窗口
建议在2026年第三季度前完成FDA Supplier Portal沙盒环境下的模块调用测试,获取官方返回的验证日志样本,用于内部技术校准与法务复核。
编辑观点 / 行业观察
Observably, this regulation is not merely a technical requirement but a strategic signal: FDA is shifting from document-centric to data-centric oversight in global supply chains. Analysis shows that the real impact lies less in upfront development cost and more in operational discipline — firms with fragmented IT systems or siloed compliance functions face higher integration friction. From industry perspective, the move accelerates the convergence of regulatory compliance, digital marketing, and procurement trust infrastructure. It is better understood as a de facto standardization push for B2B transparency, rather than an isolated audit trigger.
结语
该新规标志着监管合规正从“事后查验”迈向“事中可见”,对企业数字基建能力提出实质性检验。其长期意义不在于增设一道准入门槛,而在于推动中国出口企业将合规从法务支持职能,升级为贯穿产品全生命周期的数字化资产。理性来看,率先完成模块部署的企业,或将获得采购商优先评级、缩短验厂周期、降低质量争议举证成本等隐性竞争优势。
信息来源说明
依据美国FDA官网发布的《Guidance for Industry: Supplemental Requirements for B2B Digital Compliance Statements》(发布日期:2025年11月20日,FR Doc. No. FDA-2025-D-18742);同步参考FDA Supplier Portal技术文档v3.2(2026年4月更新版)。需持续观察FDA后续是否发布模块兼容性白名单、中小企业豁免细则及过渡期执法尺度。
相关文章
相关产品













