- Les services de marketing digital mondial à Shenzhen conviennent-ils aux entreprises qui se développent à l’internationalMay 15, 2026Voir les détails
- Quels sont les avantages des services de marketing digital mondial à ShenzhenMay 15, 2026Voir les détails
- Quelle société de conseil en marketing Internet choisir, commencez par examiner la logique de livraisonMay 15, 2026Voir les détails
- Comment l’analyse des données des agences numériques internationales soutient-elle les décisions d’investissement publicitaireMay 15, 2026Voir les détails
- Quels indicateurs clés suivre dans l’analyse des données des agences digitales internationalesMay 15, 2026Voir les détails
- Quels secteurs sont concernés par les solutions de marketing digital mondial à GuangzhouMay 15, 2026Voir les détails
- Quelles sont les nouvelles tendances des solutions de marketing digital mondial à GuangzhouMay 15, 2026Voir les détails
- Quels problèmes les services d’une société de conseil en marketing digital peuvent-ils résoudreMay 15, 2026Voir les détails
La nouvelle réglementation de la FDA américaine entre en vigueur le 15 mai : les sites web B2B doivent intégrer un module de vérification de conformité en temps réel
Le 15 mai 2026, la Food and Drug Administration (FDA) des États-Unis a officiellement mis en œuvre les clauses complémentaires du "Guide des déclarations de conformité numérique B2B". Cette politique intègre pour la première fois la capacité de présentation de la conformité numérique des sites web d’entreprise dans le système d’évaluation des qualifications de la chaîne d’approvisionnement, affectant directement l’efficacité de l’accès commercial et les bases de confiance commerciale des exportations chinoises vers les États-Unis de dispositifs médicaux, de matériaux en contact avec les aliments et de produits électroniques grand public.
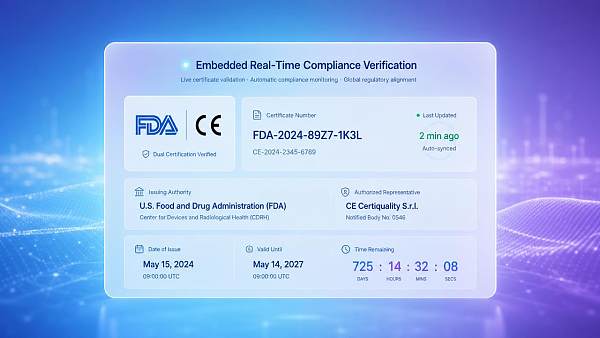
Aperçu de l’événement
Le 15 mai 2026, la FDA des États-Unis a officiellement mis en œuvre les clauses complémentaires du "Guide des déclarations de conformité numérique B2B", exigeant que tous les fournisseurs chinois exportant vers les États-Unis des dispositifs médicaux, des matériaux en contact avec les aliments et des produits électroniques grand public intègrent sur leurs sites web multilingues un module structuré de déclaration de conformité vérifiable en ligne par la FDA (incluant le statut de double marquage CE/FDA, le numéro de certificat, l’organisme émetteur et la date de validité), faute de quoi le taux d’approbation de la préqualification des acheteurs dans le FDA Supplier Portal sera affecté. Cette exigence influence directement l’évaluation de la crédibilité des fournisseurs par les importateurs étrangers ainsi que les décisions de libération des commandes.
Quels sous-secteurs seront impactés
Entreprises de commerce direct:en tant qu’entités enregistrées dans le FDA Supplier Portal et parties signataires des contrats d’achat, leurs sites web constituent la première source d’information pour les importateurs menant une due diligence. Si aucun module vérifiable n’est intégré, cela entraînera des retards dans la préqualification ou un marquage comme "informations incomplètes", allongeant considérablement le cycle d’accès des nouveaux clients, et pouvant déclencher des coûts supplémentaires tels que l’exigence par les acheteurs de fournir des rapports de vérification tiers.
Entreprises d’approvisionnement en matières premières:bien qu’elles n’exportent pas directement des produits finis, les matières premières clés qu’elles fournissent aux fabricants en aval (telles que le silicone de qualité médicale, la résine PC de qualité alimentaire, ou les puces conformes RoHS) doivent être accompagnées de preuves de conformité traçables. La nouvelle réglementation les pousse à mettre simultanément à niveau les modules de déclaration de leurs sites web afin d’aider les clients en aval à remplir leurs obligations de divulgation de conformité pour les machines/pièces complètes, faute de quoi elles risquent un affaiblissement de leurs relations d’approvisionnement.
Entreprises de fabrication sous-traitée:les entreprises assumant un rôle OEM/ODM déposent souvent l’enregistrement FDA au nom de la marque, tandis que leurs propres sites web manquent depuis longtemps d’identification de conformité indépendante. Après l’entrée en vigueur de la nouvelle réglementation, les importateurs auront davantage tendance à choisir des fabricants disposant d’une capacité autonome d’infrastructure numérique de conformité, afin de réduire les risques de responsabilité solidaire;ceux qui en sont dépourvus pourraient être exclus des listes d’achats de qualité.
Entreprises de services de chaîne d’approvisionnement:y compris les prestataires tiers de conseil en conformité, de gestion des certifications, de développement de plateformes numériques, etc., dont le modèle économique évolue de "service ponctuel de certificat" vers "exploitation et maintenance continues des données de conformité". La nouvelle réglementation accélère objectivement la pénétration du marché des outils SaaS de conformité, tout en imposant des exigences plus élevées aux prestataires en matière de capacités de structuration des données, d’expérience d’intégration API et de gestion de contenu multilingue.
Points d’attention et mesures de réponse pour les entreprises ou praticiens concernés
Vérifier si le site web répond aux normes de données structurées
Il convient de vérifier si le site web adopte les champs étendus Product et Certification de la norme Schema.org, afin de permettre au système FDA de récupérer automatiquement les paramètres clés tels que le numéro de certificat, la date de délivrance, la date de validité et l’URI de l’organisme certificateur, au lieu de se limiter à l’affichage statique de fichiers PDF numérisés.
Clarifier la cohérence des déclarations de conformité sur les pages multilingues
Le site principal en anglais et le sous-site en chinois doivent tous deux déployer des modules de vérification ayant la même valeur juridique;si seule la page anglaise est intégrée tandis que la page chinoise en est dépourvue, le système FDA peut considérer qu’il s’agit d’une "asymétrie d’information", affectant la note globale de crédibilité.
Mettre en place un mécanisme de mise à jour dynamique des certificats
Le module doit être relié de manière légère au système interne de gestion des certificats (tel que le QMS) ou à la base de données de l’organisme certificateur, afin de garantir que lorsque les certificats expirent, sont modifiés ou révoqués, la déclaration sur le site web soit actualisée simultanément, évitant ainsi que les acheteurs ne se trompent en raison d’informations obsolètes.
Réserver une fenêtre de test pour l’interface de vérification FDA
Il est recommandé d’achever avant le troisième trimestre 2026 les tests d’appel du module dans l’environnement sandbox du FDA Supplier Portal, et d’obtenir des échantillons de journaux de vérification retournés officiellement, à utiliser pour l’étalonnage technique interne et l’examen juridique.
Point de vue éditorial / Observation sectorielle
De manière observable, cette réglementation n’est pas seulement une exigence technique mais aussi un signal stratégique: la FDA passe d’une supervision centrée sur les documents à une supervision centrée sur les données dans les chaînes d’approvisionnement mondiales. L’analyse montre que l’impact réel réside moins dans le coût initial de développement que dans la discipline opérationnelle — les entreprises dotées de systèmes informatiques fragmentés ou de fonctions de conformité cloisonnées sont confrontées à davantage de frictions d’intégration. Du point de vue du secteur, cette évolution accélère la convergence entre conformité réglementaire, marketing numérique et infrastructure de confiance des achats. Elle doit plutôt être comprise comme une poussée de normalisation de facto pour la transparence B2B, plutôt que comme un déclencheur d’audit isolé.
Conclusion
Cette nouvelle réglementation marque le passage de la conformité réglementaire d’un modèle de "contrôle a posteriori" à un modèle de "visibilité en temps réel", imposant un véritable test des capacités d’infrastructure numérique des entreprises. Sa signification à long terme ne réside pas dans l’ajout d’une barrière supplémentaire à l’entrée, mais dans l’incitation des entreprises exportatrices chinoises à faire évoluer la conformité, d’une fonction de soutien juridique, vers un actif numérique couvrant l’ensemble du cycle de vie du produit. D’un point de vue rationnel, les entreprises qui achèveront en premier le déploiement du module pourraient obtenir des avantages concurrentiels implicites, tels qu’une priorisation dans l’évaluation par les acheteurs, un raccourcissement des cycles d’audit d’usine et une réduction des coûts de preuve dans les litiges qualité.
Description de la source d’information
Sur la base du document publié sur le site officiel de la FDA des États-Unis, "Guide de l’industrie: Exigences complémentaires pour les déclarations de conformité numérique B2B" (date de publication:20 novembre 2025, FR Doc. No. FDA-2025-D-18742);référence simultanée à la documentation technique v3.2 du FDA Supplier Portal (mise à jour d’avril 2026). Il convient de continuer à observer si la FDA publiera par la suite une liste blanche de compatibilité des modules, des règles d’exemption pour les PME ainsi que l’intensité d’application pendant la période transitoire.
Articles connexes
![L'UE met à jour le règlement sur l'interopérabilité des services numériques, les plateformes chinoises de création de sites SaaS doivent ouvrir leurs API L'UE met à jour le règlement sur l'interopérabilité des services numériques, les plateformes chinoises de création de sites SaaS doivent ouvrir leurs API]() L'UE met à jour le règlement sur l'interopérabilité des services numériques, les plateformes chinoises de création de sites SaaS doivent ouvrir leurs API
L'UE met à jour le règlement sur l'interopérabilité des services numériques, les plateformes chinoises de création de sites SaaS doivent ouvrir leurs API![Les machines laser sont plus prisées pour l’acquisition de clients à l’étranger sur Google Les machines laser sont plus prisées pour l’acquisition de clients à l’étranger sur Google]() Les machines laser sont plus prisées pour l’acquisition de clients à l’étranger sur Google
Les machines laser sont plus prisées pour l’acquisition de clients à l’étranger sur Google![Google n’est pas de la magie, c’est juste un amplificateur ! Google n’est pas de la magie, c’est juste un amplificateur !]() Google n’est pas de la magie, c’est juste un amplificateur !
Google n’est pas de la magie, c’est juste un amplificateur !
Produits associés













