- ¿Es adecuado el servicio global de marketing digital de Shenzhen para las empresas que buscan expandirse al extranjero?15-05-2026Ver detalles
- ¿Cuáles son las ventajas de los servicios de marketing digital global en Shenzhen?15-05-2026Ver detalles
- ¿Qué empresa de consultoría de marketing en Internet es mejor? Primero, fíjese en la lógica de entrega15-05-2026Ver detalles
- Cómo el análisis de datos de las agencias digitales internacionales respalda las decisiones de inversión publicitaria15-05-2026Ver detalles
- ¿Qué indicadores clave deben analizarse en los datos de agencias digitales internacionales?15-05-2026Ver detalles
- ¿Para qué sectores es adecuada la solución de marketing digital global de Guangzhou?15-05-2026Ver detalles
- ¿Cuáles son las nuevas tendencias en las soluciones de marketing digital global en Guangzhou?15-05-2026Ver detalles
- ¿Qué problemas pueden resolver los servicios de una empresa de consultoría de marketing digital?15-05-2026Ver detalles
La nueva normativa de la FDA de EE. UU. entra en vigor el 15 de mayo: los sitios web B2B deben integrar módulos de verificación de cumplimiento en tiempo real
El 15 de mayo de 2026, la Administración de Alimentos y Medicamentos de Estados Unidos(FDA)implementó oficialmente las disposiciones complementarias de la "Guía de Declaraciones de Cumplimiento Digital B2B". Esta política incorporó por primera vez la capacidad de presentación del cumplimiento digital de los sitios web corporativos al sistema de evaluación de calificación de la cadena de suministro, afectando directamente la eficiencia de acceso comercial y la base de confianza comercial de las exportaciones chinas a Estados Unidos de dispositivos médicos, materiales en contacto con alimentos y productos de electrónica de consumo.
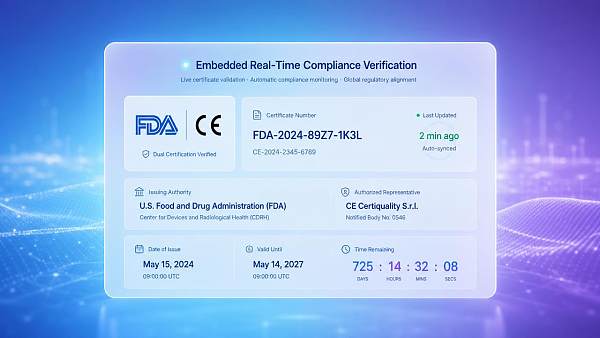
Resumen del evento
El 15 de mayo de 2026, la FDA de Estados Unidos implementó oficialmente las disposiciones complementarias de la "Guía de Declaraciones de Cumplimiento Digital B2B", exigiendo que todos los proveedores chinos que exporten a Estados Unidos dispositivos médicos, materiales en contacto con alimentos y productos de electrónica de consumo integren en sus sitios web multilingües módulos estructurados de declaraciones de cumplimiento verificables en línea por la FDA(incluido el estado de doble marcado CE/FDA, número de certificado, organismo emisor y período de validez), de lo contrario se verá afectada la tasa de aprobación de la precalificación de los compradores en el FDA Supplier Portal. Este requisito afecta directamente la evaluación de credibilidad de los proveedores por parte de los importadores extranjeros y las decisiones de liberación de pedidos.
Qué subsectores se verán afectados
Empresas de comercio directo:como entidades registradas en el FDA Supplier Portal y partes firmantes de contratos de compra, sus sitios web son la primera fuente de información para que los importadores realicen la diligencia debida. Si no incorporan módulos verificables, esto provocará retrasos en la precalificación o la marca de “información incompleta”, alargando significativamente el ciclo de acceso de nuevos clientes, y también puede activar costos adicionales como la exigencia por parte del comprador de aportar informes de verificación de terceros.
Empresas de compra de materias primas:aunque no exportan directamente productos terminados, las materias primas clave que suministran a los fabricantes aguas abajo(como silicona de grado médico, resina PC de grado alimentario y chips conformes con RoHS)deben ir acompañadas de pruebas de cumplimiento rastreables. La nueva normativa obliga a actualizar de forma sincronizada los módulos de declaración de sus sitios web para apoyar a los clientes aguas abajo en el cumplimiento de las obligaciones de divulgación de conformidad de equipos completos/componentes completos, de lo contrario se enfrentarán al riesgo de debilitamiento de las relaciones de suministro.
Empresas de procesamiento y fabricación:las empresas que asumen funciones OEM/ODM suelen solicitar el registro FDA a nombre de la marca, mientras que sus propios sitios web han carecido durante mucho tiempo de identificaciones de cumplimiento independientes. Tras la entrada en vigor de la nueva normativa, los importadores tenderán más a elegir fabricantes con capacidad propia de infraestructura digital de cumplimiento, para reducir el riesgo de responsabilidad solidaria;quienes carezcan de esta capacidad podrían quedar excluidos de las listas de compras de alta calidad.
Empresas de servicios de cadena de suministro:incluidos proveedores externos de servicios como consultoría de cumplimiento, gestión de certificaciones y desarrollo de plataformas digitales, cuyo modelo de negocio está pasando de “servicios puntuales de certificación” a “operación y mantenimiento continuos de datos de cumplimiento”. La nueva normativa acelera objetivamente la penetración de mercado de las herramientas SaaS de cumplimiento, y también plantea mayores exigencias a la capacidad de estructuración de datos de los proveedores de servicios, la experiencia en integración de API y la gestión de contenidos multilingües.
Puntos clave de atención y medidas de respuesta para empresas o profesionales relacionados
Confirmar si el sitio web cumple con las normas de datos estructurados
Es necesario verificar si el sitio web adopta los campos extendidos de Product y Certification del estándar Schema.org, para permitir que el sistema de la FDA capture automáticamente parámetros clave como número de certificado, fecha de emisión, período de validez y URI del organismo certificador, en lugar de limitarse a mostrar archivos PDF escaneados estáticos.
Aclarar la coherencia de las declaraciones de cumplimiento en páginas multilingües
Tanto el sitio principal en inglés como el subsitio en chino deben implementar módulos de verificación con la misma validez;si solo la página en inglés está integrada y la página en chino carece de ello, el sistema de la FDA puede determinar que existe “asimetría de información”, afectando la puntuación general de credibilidad.
Establecer un mecanismo de actualización dinámica de certificados
El módulo debe lograr una integración ligera con el sistema interno de gestión de certificados(como QMS)o la base de datos del organismo certificador, para garantizar que cuando un certificado expire, cambie o sea revocado, la declaración del sitio web se actualice de forma sincronizada, evitando errores de juicio de los compradores por información desactualizada.
Reservar una ventana de prueba para la interfaz de verificación de la FDA
Se recomienda completar antes del tercer trimestre de 2026 las pruebas de llamada del módulo en el entorno sandbox del FDA Supplier Portal, obteniendo muestras de registros de verificación devueltas oficialmente, para utilizarlas en la calibración técnica interna y la revisión legal.
Opinión editorial / Observación del sector
Evidentemente, esta regulación no es solo un requisito técnico, sino también una señal estratégica: la FDA está pasando de una supervisión centrada en documentos a una supervisión centrada en datos en las cadenas de suministro globales. El análisis muestra que el verdadero impacto reside menos en el costo inicial de desarrollo y más en la disciplina operativa — las empresas con sistemas de TI fragmentados o funciones de cumplimiento aisladas afrontan una mayor fricción de integración. Desde la perspectiva del sector, esta medida acelera la convergencia entre el cumplimiento normativo, el marketing digital y la infraestructura de confianza en compras. Se entiende mejor como un impulso de estandarización de facto para la transparencia B2B, más que como un desencadenante aislado de auditoría.
Conclusión
Esta nueva normativa marca que el cumplimiento regulatorio está pasando de la “inspección posterior” a la “visibilidad durante el proceso”, planteando una prueba sustancial para la capacidad de infraestructura digital de las empresas. Su significado a largo plazo no radica en añadir una barrera más de acceso, sino en impulsar a las empresas exportadoras chinas a actualizar el cumplimiento desde una función de apoyo legal hasta un activo digital que atraviese todo el ciclo de vida del producto. Racionalmente, las empresas que completen primero la implementación de módulos podrían obtener ventajas competitivas implícitas como prioridad en la calificación de compradores, reducción del ciclo de auditoría de fábrica y disminución del costo probatorio en disputas de calidad.
Descripción de la fuente de información
Según la "Guía para la Industria: Requisitos Complementarios para Declaraciones de Cumplimiento Digital B2B" publicada en el sitio web oficial de la FDA de Estados Unidos(fecha de publicación:20 de noviembre de 2025, FR Doc. No. FDA-2025-D-18742);también se consultó de forma simultánea la documentación técnica v3.2 del FDA Supplier Portal(versión actualizada de abril de 2026). Es necesario seguir observando si la FDA publicará posteriormente una lista blanca de compatibilidad de módulos, detalles de exención para pequeñas y medianas empresas y el alcance de la aplicación durante el período transitorio.
Artículos relacionados
Productos relacionados













