- Sind globale digitale Marketingservices in Shenzhen für Unternehmen geeignet, die ins Ausland expandieren15-05-2026Details anzeigen
- Was sind die Vorteile globaler digitaler Marketingservices in Shenzhen15-05-2026Details anzeigen
- Welche Internet-Marketing-Beratungsfirma ist gut, zuerst die Lieferlogik prüfen15-05-2026Details anzeigen
- Wie unterstützt die Datenanalyse internationaler digitaler Agenturen Anzeigenentscheidungen15-05-2026Details anzeigen
- Welche Kernkennzahlen sollte man bei der Datenanalyse internationaler Digitalagenturen betrachten15-05-2026Details anzeigen
- Für welche Branchen eignet sich die globale digitale Marketinglösung in Guangzhou15-05-2026Details anzeigen
- Welche neuen Trends gibt es bei globalen digitalen Marketinglösungen in Guangzhou15-05-2026Details anzeigen
- Welche Probleme können die Dienstleistungen einer Internet-Marketing-Beratung lösen15-05-2026Details anzeigen
Neue FDA-Vorschrift der USA tritt am 15. Mai in Kraft: B2B-Unternehmenswebsites müssen ein Modul zur Echtzeit-Compliance-Verifizierung integrieren
Am 15. Mai 2026 setzt die US-amerikanische Food and Drug Administration(FDA)offiziell die ergänzenden Bestimmungen des „Leitfadens für B2B-Erklärungen zur digitalen Compliance“ in Kraft. Diese Richtlinie bezieht erstmals die Fähigkeit zur digitalen und regelkonformen Darstellung auf Unternehmenswebsites in das Bewertungssystem für Lieferkettenqualifikationen ein und beeinflusst direkt die Effizienz des Marktzugangs sowie die Grundlage des geschäftlichen Vertrauens für chinesische Exporte von Medizinprodukten, Materialien mit Lebensmittelkontakt und Unterhaltungselektronik in die USA.
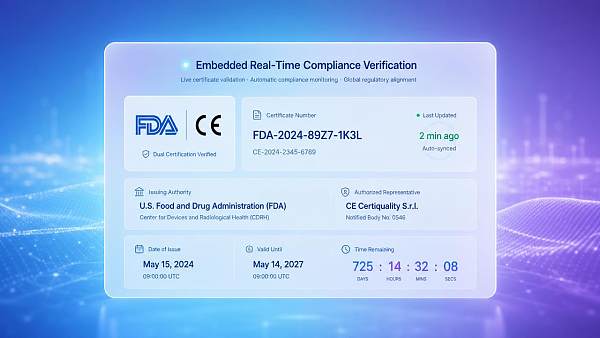
Ereignisüberblick
Die US-amerikanische FDA setzt am 15. Mai 2026 offiziell die ergänzenden Bestimmungen des „Leitfadens für B2B-Erklärungen zur digitalen Compliance“ in Kraft. Danach müssen alle chinesischen Lieferanten, die Medizinprodukte, Materialien mit Lebensmittelkontakt und Unterhaltungselektronik in die USA exportieren, auf ihren mehrsprachigen Unternehmenswebsites ein von der FDA online verifizierbares Modul für strukturierte Compliance-Erklärungen integrieren(einschließlich CE/FDA-Doppelkennzeichnungsstatus, Zertifikatsnummer, ausstellender Stelle und Gültigkeitsdauer), andernfalls wird die Erfolgsquote der Qualifikationsvorprüfung von Einkäufern im FDA Supplier Portal beeinträchtigt. Diese Anforderung wirkt sich unmittelbar auf die Bewertung der Lieferantenzuverlässigkeit durch ausländische Importeure sowie auf Entscheidungen zur Auftragsfreigabe aus.
Welche Teilbranchen betroffen sind
Direkt handelnde Unternehmen:Als im FDA Supplier Portal registrierte Einheit und Vertragspartei bei Beschaffungsverträgen ist ihre Website die erste Informationsquelle für Importeure bei der Durchführung der Due Diligence. Ist kein verifizierbares Modul eingebettet, führt dies zu Verzögerungen bei der Qualifikationsvorprüfung oder zu einer Kennzeichnung als „unvollständige Informationen“, was den Zulassungszyklus für Neukunden deutlich verlängert und möglicherweise zusätzliche Kosten auslöst, weil Einkäufer die Vorlage von Drittprüfberichten verlangen.
Unternehmen der Rohstoffbeschaffung:Obwohl sie keine Fertigprodukte direkt exportieren, müssen die von ihnen an nachgelagerte Hersteller gelieferten Schlüsselrohstoffe(wie medizinisches Silikon, lebensmitteltaugliches PC-Harz, RoHS-konforme Chips)mit rückverfolgbaren Compliance-Nachweisen versehen sein. Die neue Vorschrift zwingt sie dazu, die Erklärungsmodule auf ihren Websites synchron aufzurüsten, um nachgelagerte Kunden bei der Erfüllung ihrer Offenlegungspflichten für die Konformität kompletter Maschinen/Bauteile zu unterstützen; andernfalls besteht das Risiko einer Schwächung der Lieferbeziehung.
Verarbeitende Fertigungsunternehmen:Unternehmen in der Rolle von OEM/ODM melden FDA-Listungen häufig im Namen der Markeninhaber an, während auf ihren eigenen Websites langfristig eine eigenständige Compliance-Kennzeichnung fehlt. Nach Inkrafttreten der neuen Vorschrift werden Importeure eher Hersteller wählen, die über eigenständige digitale Grundlagen für Compliance verfügen, um das Risiko einer Mitverantwortung zu senken; wer diese Fähigkeit nicht besitzt, könnte von Listen bevorzugter Beschaffung ausgeschlossen werden.
Unternehmen für Lieferkettendienstleistungen:Dazu gehören Drittanbieter wie Compliance-Beratung, Zertifizierungsvertretung und Entwicklung digitaler Plattformen, deren Geschäftsmodell sich von „einmaligem Zertifikatsservice“ zu „kontinuierlichem Betrieb und Wartung von Compliance-Daten“ wandelt. Die neue Vorschrift beschleunigt objektiv die Marktdurchdringung von Compliance-SaaS-Tools und stellt zugleich höhere Anforderungen an die Fähigkeit der Dienstleister zur Datenstrukturierung, API-Anbindungserfahrung und Verwaltung mehrsprachiger Inhalte.
Worauf betroffene Unternehmen oder Praktiker achten sollten und Gegenmaßnahmen
Prüfen, ob die Website die Standards für strukturierte Daten erfüllt
Es ist zu prüfen, ob die Website die Erweiterungsfelder Product und Certification des Schema.org-Standards verwendet, damit das FDA-System zentrale Parameter wie Zertifikatsnummer, Ausstellungsdatum, Gültigkeitsdauer und URI der Zertifizierungsstelle automatisch erfassen kann, anstatt lediglich statische PDF-Scans anzuzeigen.
Konsistenz der Compliance-Erklärungen auf mehrsprachigen Seiten klären
Sowohl die englische Hauptseite als auch die chinesische Unterseite müssen mit gleichwertigen Verifizierungsmodulen ausgestattet sein; ist nur die englische Seite eingebettet, während die chinesische Seite fehlt, kann das FDA-System dies möglicherweise als „asymmetrische Informationen“ einstufen, was die Gesamtbewertung der Vertrauenswürdigkeit beeinträchtigt.
Mechanismus zur dynamischen Aktualisierung von Zertifikaten einrichten
Das Modul muss leichtgewichtig an interne Zertifikatsmanagementsysteme(wie QMS)oder Datenbanken von Zertifizierungsstellen angebunden werden, um sicherzustellen, dass bei Ablauf, Änderung oder Widerruf von Zertifikaten die Erklärung auf der Website synchron aktualisiert wird und Fehleinschätzungen von Einkäufern aufgrund veralteter Informationen vermieden werden.
Testfenster für die FDA-Verifizierungsschnittstelle vorsehen
Es wird empfohlen, vor dem 3. Quartal 2026 den Modultest in der Sandbox-Umgebung des FDA Supplier Portal abzuschließen und offizielle Muster der Verifizierungsprotokolle zu erhalten, die für interne technische Kalibrierung und rechtliche Prüfung verwendet werden können.
Redaktionelle Sicht / Branchenbeobachtung
Offensichtlich ist diese Verordnung nicht nur eine technische Anforderung, sondern auch ein strategisches Signal: Die FDA verlagert ihre Aufsicht in globalen Lieferketten von einer dokumentenzentrierten zu einer datenorientierten Kontrolle. Die Analyse zeigt, dass die tatsächlichen Auswirkungen weniger in den anfänglichen Entwicklungskosten liegen als vielmehr in der operativen Disziplin — Unternehmen mit fragmentierten IT-Systemen oder voneinander isolierten Compliance-Funktionen sind mit höheren Integrationshürden konfrontiert. Aus Branchensicht beschleunigt dieser Schritt die Konvergenz von regulatorischer Compliance, digitalem Marketing und Vertrauensinfrastruktur im Beschaffungswesen. Er ist besser als faktischer Standardisierungsschub für B2B-Transparenz zu verstehen denn als isolierter Auslöser für Prüfungen.
Fazit
Die neue Vorschrift kennzeichnet, dass sich die regulatorische Compliance von „nachträglicher Prüfung“ hin zu „Sichtbarkeit während des Prozesses“ bewegt, und stellt die digitalen Grundlagenfähigkeiten von Unternehmen auf eine substanzielle Probe. Ihre langfristige Bedeutung liegt nicht darin, eine weitere Marktzugangshürde zu schaffen, sondern darin, chinesische Exportunternehmen dazu zu bewegen, Compliance von einer rechtlichen Unterstützungsfunktion zu einem digitalen Vermögenswert aufzuwerten, der den gesamten Produktlebenszyklus durchdringt. Rational betrachtet könnten Unternehmen, die die Modulbereitstellung zuerst abschließen, versteckte Wettbewerbsvorteile erlangen, etwa durch bevorzugte Bewertung durch Einkäufer, verkürzte Werksaudit-Zyklen und geringere Beweiskosten bei Qualitätsstreitigkeiten.
Hinweis zu den Informationsquellen
Grundlage sind der auf der offiziellen Website der US-amerikanischen FDA veröffentlichte „Leitfaden für die Industrie: Ergänzende Anforderungen an B2B-Erklärungen zur digitalen Compliance“(Veröffentlichungsdatum:20. November 2025, FR Doc. No. FDA-2025-D-18742)sowie ergänzend die technische Dokumentation des FDA Supplier Portal v3.2(aktualisierte Fassung vom April 2026). Es ist weiterhin zu beobachten, ob die FDA nachfolgend eine Whitelist zur Modulkompatibilität, detaillierte Ausnahmeregelungen für kleine und mittlere Unternehmen sowie den Durchsetzungsrahmen während der Übergangsfrist veröffentlicht.
Verwandte Artikel
Verwandte Produkte













