- 深圳のグローバルデジタルマーケティングサービスは海外進出企業に適していますか15/05/2026詳細を見る
- 深センのグローバルデジタルマーケティングサービスの強みとは15/05/2026詳細を見る
- どのインターネットマーケティングコンサルティング会社が良いか,まずはデリバリーロジックを見る15/05/2026詳細を見る
- 国際的なデジタル機関のデータ分析はどのように配信意思決定を支援するか15/05/2026詳細を見る
- 国際デジタル機関のデータ分析ではどの中核指標を見るべきか15/05/2026詳細を見る
- 広州のグローバルデジタルマーケティングソリューションはどのような業界に適していますか15/05/2026詳細を見る
- 広州のグローバルデジタルマーケティングソリューションにはどのような新たなトレンドがあるのか15/05/2026詳細を見る
- インターネットマーケティングコンサルティング会社のサービスで解決できる課題15/05/2026詳細を見る
米国FDA新規則5月15日施行:B2B公式サイトにはリアルタイムコンプライアンス検証モジュールの組み込みが必須
2026年5月15日, 米国食品医薬品局(FDA)は「B2Bデジタルコンプライアンス声明ガイドライン」の補足条項を正式に施行しました。この政策は初めて、企業公式サイトにおけるデジタル化されたコンプライアンス表示能力をサプライチェーンの資格評価体系に組み込み、中国から米国へ輸出される医療機器, 食品接触材料および消費者向け電子製品の取引参入効率と商業的信頼基盤に直接影響を及ぼします。
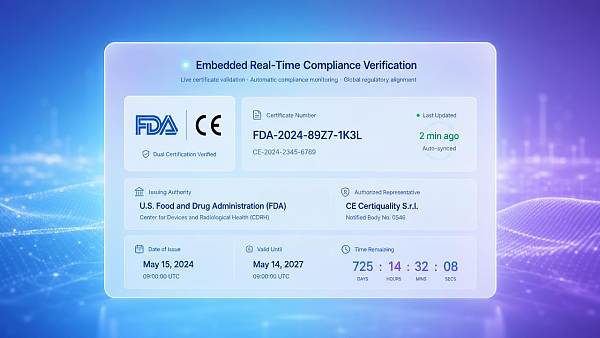
事案概要
米国FDAは2026年5月15日に「B2Bデジタルコンプライアンス声明ガイドライン」の補足条項を正式に施行し, 米国向けに医療機器, 食品接触材料および消費者向け電子製品を輸出するすべての中国サプライヤーに対し, その多言語公式サイトにFDAがオンラインで検証可能な構造化コンプライアンス声明モジュール(CE/FDA両規格のステータス, 証明書番号, 発行機関および有効期限を含む)を統合することを求めています。これを満たさない場合, 購買者のFDA Supplier Portalにおける資格事前審査の通過率に影響します。この要件は, 海外輸入業者によるサプライヤー信頼性評価と発注承認判断に直接影響します。
どの細分業界に影響するか
直接貿易企業:FDA Supplier Portalにおける登録主体および購買契約の締結当事者として, その公式サイトは輸入業者がデューデリジェンスを実施する際の第一の情報源です。検証可能なモジュールが組み込まれていない場合, 資格事前審査の遅延や「情報不完全」としてマークされる原因となり, 新規顧客の参入サイクルを著しく長引かせ, さらに購買者から第三者検証レポートの提出を求められるなどの追加コストが発生する可能性があります。
原材料調達企業:完成品を直接輸出しない場合でも, 下流製造業者に供給する重要原材料(医療用グレードシリコーン, 食品グレードPC樹脂, RoHS準拠チップなど)には追跡可能なコンプライアンス証明の添付が必要です。新規制により, 下流顧客が完成機器/完成部品のコンプライアンス開示義務を果たせるよう, 公式サイト上の声明モジュールを同期的に高度化することが迫られ, さもなければ供給関係の弱体化リスクに直面します。
加工製造企業:OEM/ODMの役割を担う企業は, ブランドオーナー名義でFDA登録を申請することが多い一方, 自社公式サイトでは長期にわたり独立したコンプライアンス表示が欠けていることがあります。新規制施行後は, 輸入業者は連帯責任リスクを低減するため, 自主的なコンプライアンス向けデジタル基盤構築能力を備えた製造業者をより選好する傾向が強まり, その能力を欠く企業は優良調達リストから除外される可能性があります。
サプライチェーンサービス企業:コンプライアンスコンサルティング, 認証代行, デジタルプラットフォーム開発などの第三者サービス事業者を含み, その事業モデルは「単発の証明書サービス」から「継続的なコンプライアンスデータ運用保守」へと移行しています。新規制は客観的にコンプライアンスSaaSツールの市場浸透を加速させるとともに, サービス事業者のデータ構造化能力, API連携経験および多言語コンテンツ管理に対してより高い要件を提示しています。
関連企業または実務担当者が注目すべき重点と対応策
公式サイトが構造化データ仕様を満たしているか確認する
公式サイトがSchema.org標準のProductおよびCertification拡張フィールドを採用し, FDAシステムによる証明書番号, 発行日, 有効期限, 認証機関URIなどの中核パラメータの自動取得をサポートしているかを確認する必要があります。単なるPDFスキャンの静的表示では不十分です。
多言語ページにおけるコンプライアンス声明の一貫性を明確化する
英語メインサイトと中国語サブサイトの双方に, 同等の効力を持つ検証モジュールを実装しなければなりません。英語ページのみに組み込み, 中国語ページに欠落がある場合, FDAシステムに「情報の非対称」と判断され, 全体的な信頼性スコアに影響する可能性があります。
証明書の動的更新メカニズムを構築する
モジュールは社内証明書管理システム(QMSなど)または認証機関データベースと軽量連携を実現し, 証明書の期限切れ, 変更または取消時に, 公式サイト上の声明が同期的に更新されるよう確保し, 情報遅延による購買者の誤判断を回避する必要があります。
FDA検証インターフェースのテストウィンドウを確保する
2026年第3四半期までにFDA Supplier Portalのサンドボックス環境でモジュール呼び出しテストを完了し, 公式に返却される検証ログのサンプルを取得して, 社内技術校正および法務レビューに活用することが推奨されます。
編集部の見解 / 業界観察
明らかに, この規制は単なる技術要件ではなく, 戦略的シグナルでもあります。FDAはグローバルサプライチェーンにおける監督を, 文書中心からデータ中心へと移行させています。分析によれば, 真の影響は初期開発コストよりも運用規律にあり, ITシステムが分断されている企業やコンプライアンス機能が縦割り化している企業ほど, 統合時の摩擦が大きくなります。業界の観点から見ると, この動きは規制コンプライアンス, デジタルマーケティング, 調達信頼インフラの融合を加速させています。これは孤立した監査トリガーというより, B2B透明性に対する事実上の標準化推進として理解するほうが適切です。
結び
この新規制は, 規制コンプライアンスが「事後検査」から「過程の可視化」へと進むことを示しており, 企業のデジタル基盤構築能力に対して実質的な試金石を突きつけています。その長期的意義は参入障壁を1つ増やすことではなく, 中国の輸出企業に対して, コンプライアンスを法務支援機能から, 製品ライフサイクル全体を貫くデジタル資産へと高度化させることを促す点にあります。理性的に見れば, 率先してモジュール導入を完了した企業は, 購買者からの優先評価, 工場監査サイクルの短縮, 品質紛争における立証コストの低減など, 潜在的な競争優位を得る可能性があります。
情報源の説明
米国FDA公式サイトで公表された「業界向けガイダンス:B2Bデジタルコンプライアンス声明に関する補足要件」(公表日:2025年11月20日, FR Doc. No. FDA-2025-D-18742)に基づき, あわせてFDA Supplier Portal技術文書v3.2(2026年4月更新版)を参照しています。FDAが今後, モジュール互換性ホワイトリスト, 中小企業向け免除細則および移行期間中の執行基準を公表するかどうかについて, 継続的な観察が必要です。
関連記事
関連製品













