- Подходят ли услуги глобального цифрового маркетинга в Шэньчжэне для компаний, выходящих на зарубежные рынкиMay 15, 2026Подробнее
- Каковы преимущества глобальных услуг цифрового маркетинга в ШэньчжэнеMay 15, 2026Подробнее
- Какая компания по интернет-маркетинговому консалтингу лучше, сначала смотрите на логику реализацииMay 15, 2026Подробнее
- Как анализ данных международных цифровых агентств поддерживает решения по размещению рекламыMay 15, 2026Подробнее
- Какие ключевые показатели следует учитывать при анализе данных международных digital-агентствMay 15, 2026Подробнее
- Для каких отраслей подходит глобальное решение цифрового маркетинга в ГуанчжоуMay 15, 2026Подробнее
- Какие новые тенденции существуют в глобальных решениях цифрового маркетинга в ГуанчжоуMay 15, 2026Подробнее
- Какие проблемы решают услуги консалтинговой компании в сфере интернет-маркетингаMay 15, 2026Подробнее
Новый регламент FDA США вступает в силу 15 мая: на B2B-официальном сайте должен быть встроен модуль проверки соответствия в режиме реального времени
15日5月2026 года, Управление по контролю за продуктами и лекарствами США(FDA)официально ввело в действие дополнительные положения к «Руководству по заявлениям о цифровом соответствии B2B». Данная политика впервые включает способность цифрового представления соответствия на корпоративных сайтах в систему оценки квалификации поставщиков в цепочке поставок, напрямую влияя на эффективность допуска к торговле и основу коммерческого доверия для экспортируемых из Китая в США медицинских изделий, материалов, контактирующих с пищевыми продуктами, а также потребительской электроники.
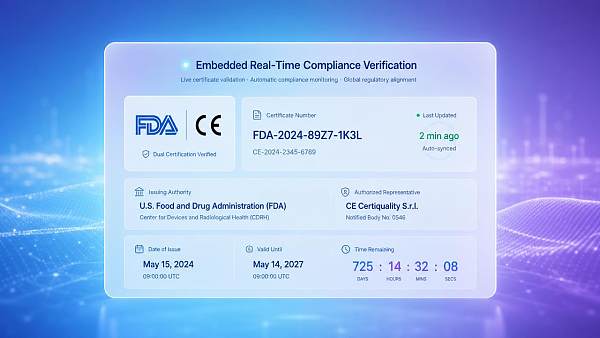
Обзор события
FDA США 15日5月2026 года официально ввело в действие дополнительные положения к «Руководству по заявлениям о цифровом соответствии B2B», требуя, чтобы все китайские поставщики, экспортирующие в США медицинские изделия, материалы, контактирующие с пищевыми продуктами, а также потребительскую электронику, интегрировали на своих многоязычных корпоративных сайтах структурированный модуль заявления о соответствии, подлежащий онлайн-проверке FDA(включая статус двойной маркировки CE/FDA, номер сертификата, орган выдачи и срок действия), в противном случае это повлияет на процент прохождения предварительной квалификационной проверки закупщиками в FDA Supplier Portal. Данное требование напрямую влияет на оценку надежности поставщика зарубежными импортерами и решения о выпуске заказов.
На какие сегменты отрасли это оказывает влияние
Предприятия прямой торговли:как зарегистрированная сторона в FDA Supplier Portal и сторона, подписывающая договор закупки, их сайт является первым источником информации для проведения импортерами due diligence. При отсутствии встроенного проверяемого модуля это приведет к задержке предварительной квалификационной проверки или маркировке как «информация неполная», что существенно удлинит цикл допуска новых клиентов и может вызвать дополнительные расходы, такие как требование закупщика предоставить отчет о сторонней проверке.
Предприятия по закупке сырья:хотя они не экспортируют готовую продукцию напрямую, ключевое сырье, поставляемое ими downstream-производителям(например, медицинский силикон, пищевой поликарбонатный PC-полимер, чипы, соответствующие RoHS), должно сопровождаться прослеживаемыми подтверждениями соответствия. Новые правила вынуждают их синхронно модернизировать модуль заявлений на сайте, чтобы поддержать выполнение downstream-клиентами обязательств по раскрытию соответствия готовых изделий/компонентов, в противном случае возникает риск ослабления отношений поставки.
Перерабатывающие и производственные предприятия:предприятия, выполняющие роль OEM/ODM, часто подают заявку на включение в список FDA от имени бренда, при этом на их собственных сайтах долгое время отсутствует независимая маркировка соответствия. После вступления новых правил в силу импортеры будут в большей степени склоняться к выбору производителей, обладающих собственной цифровой инфраструктурой соответствия, чтобы снизить риск солидарной ответственности;те, у кого такой способности нет, могут быть исключены из списка приоритетных закупок.
Предприятия услуг для цепочки поставок:включая сторонних поставщиков услуг по консультированию в области соответствия, сопровождению сертификации, разработке цифровых платформ и т.д., их бизнес-модель переходит от «разовой услуги по сертификату» к «непрерывной эксплуатации и обслуживанию данных соответствия». Новые правила объективно ускоряют проникновение на рынок SaaS-инструментов соответствия, а также выдвигают более высокие требования к способности поставщиков услуг к структурированию данных, опыту API-интеграции и управлению многоязычным контентом.
Ключевые аспекты, на которые следует обратить внимание соответствующим компаниям или специалистам, и меры реагирования
Проверить, соответствует ли сайт требованиям к структурированным данным
Необходимо проверить, использует ли сайт поля расширения Product и Certification в стандарте Schema.org, поддерживая автоматическое извлечение системой FDA таких ключевых параметров, как номер сертификата, дата выдачи, срок действия и URI органа сертификации, а не только статическое отображение PDF-сканов.
Уточнить согласованность заявлений о соответствии на многоязычных страницах
И англоязычный основной сайт, и китайский дочерний сайт должны иметь развернутые модули проверки с одинаковой юридической силой;если модуль встроен только на английской странице, а на китайской странице отсутствует, система FDA может определить это как «асимметрия информации», что повлияет на общую оценку надежности.
Создать механизм динамического обновления сертификатов
Модуль должен быть легко интегрирован с внутренней системой управления сертификатами(например, QMS)или базой данных сертифицирующего органа, чтобы при истечении срока действия сертификата, его изменении или отзыве заявление на сайте синхронно обновлялось, избегая ошибочных суждений закупщиков из-за устаревшей информации.
Заранее зарезервировать окно тестирования интерфейса проверки FDA
Рекомендуется до третьего квартала 2026 года завершить тестирование вызова модуля в sandbox-среде FDA Supplier Portal и получить образец журнала проверки, возвращаемого официальной системой, для внутренней технической калибровки и юридической проверки.
Мнение редакции / Наблюдение за отраслью
Очевидно, что данное регулирование является не просто техническим требованием, а стратегическим сигналом: FDA переходит от надзора, ориентированного на документы, к надзору, ориентированному на данные, в глобальных цепочках поставок. Анализ показывает, что реальное влияние заключается не столько в первоначальных затратах на разработку, сколько в операционной дисциплине — компании с фрагментированными IT-системами или разобщенными функциями compliance сталкиваются с более высоким трением интеграции. С отраслевой точки зрения этот шаг ускоряет сближение регуляторного соответствия, цифрового маркетинга и инфраструктуры доверия в закупках. Это лучше понимать как фактическое продвижение стандартизации прозрачности B2B, а не как изолированный триггер аудита.
Заключение
Данное новое правило знаменует переход регуляторного соответствия от «проверки постфактум» к «видимости в процессе», выдвигая содержательную проверку цифровой инфраструктурной способности предприятий. Его долгосрочное значение заключается не в добавлении еще одного порога доступа, а в стимулировании китайских экспортных предприятий к повышению роли compliance из функции юридической поддержки до цифрового актива, проходящего через весь жизненный цикл продукта. Рационально оценивая ситуацию, предприятия, которые первыми завершат развертывание модуля, возможно, получат скрытые конкурентные преимущества, такие как приоритетная оценка со стороны закупщиков, сокращение цикла аудита завода и снижение издержек на доказывание в спорах о качестве.
说明 об источнике информации
Согласно опубликованному на официальном сайте FDA США документу «Руководство для отрасли: Дополнительные требования к заявлениям о цифровом соответствии B2B»(дата публикации:20日11月2025 года, FR Doc. No. FDA-2025-D-18742);одновременно использовалась техническая документация FDA Supplier Portal v3.2(обновленная версия от апреля 2026 года). Необходимо продолжать наблюдать, выпустит ли FDA в дальнейшем белый список совместимости модулей, подробные правила освобождения для малых и средних предприятий, а также стандарты правоприменения в переходный период.
Связанные статьи
Связанные продукты













